Cell:新研究表明AOAH增强多种癌症免疫疗法,有望开发出新的免疫疗法
来源:生物谷原创 2025-11-25 10:34
该研究系统揭示了AOAH增强抗肿瘤免疫的独特分子机制。这种分泌性脂肪酶能够清除肿瘤微环境中抑制免疫应答的特定磷脂酰胆碱分子。
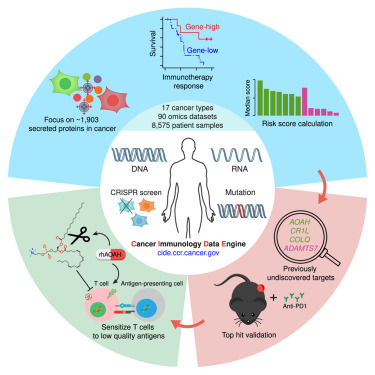
我国香港大学李嘉诚医学院临床肿瘤学系及癌症医学中心研究团队,与美国国家癌症研究所(NCI)合作,成功开发创新大数据平台"癌症免疫学数据引擎(Cancer Immunology Data Engine, CIDE)"。该平台整合了全球5,957名接受免疫治疗的癌症患者的临床结果,涵盖17种癌症类型的全面多组学数据集,包含8,575个肿瘤样本。该研究已发表于《细胞》杂志。

CIDE是迄今为止最全面的肿瘤免疫治疗数据库。该平台目前已通过NCI网站向全球研究人员开放,支持深入探索和分析临床试验数据,从而加速癌症免疫治疗研究的进展。
港大临床医学学院癌症医学中心临床肿瘤学系主任及夏碧川·沈月明癌症研究教授Guan Xinyuan教授,与NCI的Jiang Peng博士共同指出:"人类基因组中约有1,903个编码分泌蛋白的基因,其中61%在癌症发展中的功能尚未明确。
"通过应用CIDE,我们团队进行了全面分析,鉴定出与泛癌免疫治疗结果密切相关的基因,包括多个此前未被认识到与癌症相关的分泌蛋白。其中,酰基酰氧基水解酶(acyloxyacyl hydrolase, AOAH)脱颖而出,成为最突出的候选因子,在黑色素瘤、胰腺癌、肝细胞癌、结直肠癌和肾癌等多种肿瘤类型中展现出显著的免疫治疗潜力。"
AOAH如何激活免疫系统靶向癌细胞
该研究系统揭示了AOAH增强抗肿瘤免疫的独特分子机制。这种分泌性脂肪酶能够清除肿瘤微环境中抑制免疫应答的特定磷脂酰胆碱分子。这一作用有助于恢复和加强免疫系统抗击癌症的能力,特别是通过增强CD8+ T细胞的活化和肿瘤杀伤能力,同时帮助树突状细胞恢复其抗原呈递和启动免疫应答的能力。
值得注意的是,大多数晚期肿瘤通过降低其抗原可见性和免疫原性来逃避免疫监视,这对晚期癌症患者的免疫治疗构成了重大挑战。AOAH通过直接解决这一问题,成为克服晚期癌症免疫逃逸的关键调节因子。
AOAH增强多种癌症免疫疗法
在黑色素瘤、肝细胞癌和肾癌的小鼠模型中,AOAH与免疫检查点抑制剂或TCR-T细胞疗法联用显著延长了小鼠存活期。
瘤内注射AOAH蛋白也产生了强大的免疫激活效果,并与抗PD-1和抗CTLA-4治疗联用显示出协同效益,凸显了其增强多种治疗方案的能力。从机制上讲,AOAH促进了关键免疫细胞(特别是CD8+ T细胞和CD11+树突状细胞)向肿瘤微环境的浸润。
这些细胞对于抗原识别、免疫信号传递和免疫激活至关重要,而这些过程对免疫治疗的成功至关重要。AOAH不仅展示出独立的治疗潜力,还能作为现有免疫疗法的有力补充,为克服晚期癌症的免疫耐药性提供了前景广阔的策略。
AOAH作为联合治疗中的新型抗癌模式
分泌蛋白在细胞间通讯和免疫调节中发挥着关键作用。其扩散效应能够在肿瘤微环境、淋巴结和免疫器官中协调免疫应答。
基于这一原理,研究团队正在设计将AOAH与PD-L1抗体结合的抗体偶联药物,提供能够同时靶向肿瘤细胞及其微环境的下一代精准免疫疗法。
小鼠模型的临床前研究将评估这种方法的疗效、安全性及作用模式。
Guan教授表示:"我们目前正在推进早期临床试验,目标是將难治性晚期癌症患者的治愈率从当前的5–20%提升至40%以上。依托粤港澳大湾区的战略优势,我们致力于将这一创新成果推向全球,惠及世界各地的癌症患者。"(生物谷Bioon.com)
参考文献:
Lanqi Gong et al, Cancer immunology data engine reveals secreted AOAH as a potential immunotherapy, Cell (2025). DOI: 10.1016/j.cell.2025.07.004.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


